
3-2
熱對物質的影響
3-2-1
物態變化
◎
粒子模型解釋三態變化
◎
溫度與三態變化、潛熱
◎
壓力對熔點、沸點的影響
◎
蒸發與昇華
3-2-2
熱膨脹
◎
熱脹冷縮現象
◎
熱膨脹的生活應用
◎
水的熱膨脹性質
3-2-1 物態變化
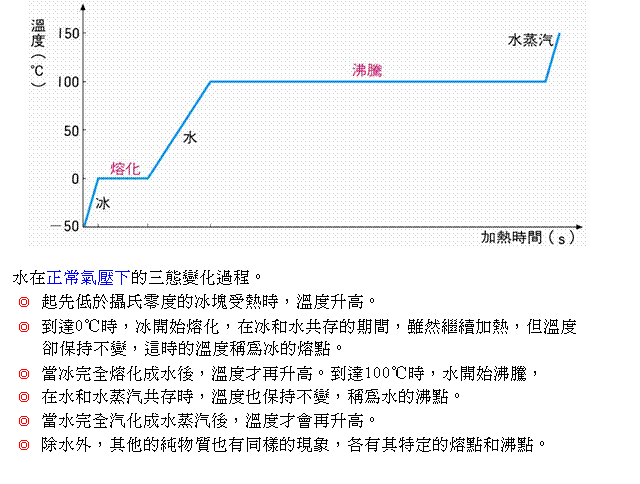
物體受熱後溫度升高,或冷卻後溫度降低,至某一程度時,其形態會發生變化,例如固態的冰受熱後,熔化成液態的水;若再繼續加熱,則水經由蒸發或沸騰的過程,轉變為氣態的水蒸汽。這些形態的改變稱為物態變化。
自然界的物質,在不同條件下,可以三種物態存在,即固態、液態、氣態。岩石在平常狀況下為固態,但火山爆發時所噴出的岩漿,顯示岩石在地核高溫下是處於液態。即使是空氣也可冷卻成液態,或甚至進一步冷卻成固態。
粒子模型解釋三態變化
物質的三態變化,可以利用物質的粒子模型予以解釋。所謂粒子指的是組成物質的眾多分子或原子。這些粒子之間,彼此有互相作用的力,統稱為分子力。
分子力的大小和方向與兩分子間的距離有關:當分子間的距離變大時,產生吸引作用;反之,距離變小時,產生排斥作用。因此分子間維持在一個適當的平衡距離。
分子力的性質很像是彈簧的恢復力:當彈簧被拉長時,產生向內的拉力;而當被壓縮時,產生向外的推力。但是當分子之間的距離過大時,分子力的大小隨距離的增加而迅速地減弱。
固體內的分子之間彼此吸引牽制,呈現有規則的排列,但各分子並不是固定不動,而是在各自的平衡位置附近做零亂的微小振動。由於分子力的強力束縛,使固體不易變形,因此固體具有一定的形狀與體積。分子振動速度的快慢代表溫度的高低。換句話說,溫度是反映分子運動的激烈程度。

對固體加熱使其溫度升高時,分子振動的速度加快,振動的幅度變大,分子間的距離也隨之增加,分子力的束縛相對地減弱。
熔化
如果溫度夠高,有些分子的速度將加快致使分子力無法再將其拘束在固定位置,而形成許多分離的分子團,轉變成液體。固體解離成液體的相變過程,稱為熔化。分子在液體中可以相當自由地移動,但減弱的分子力仍足以使它們牽連在一起,因此液體雖無固定的形狀,但仍具有一定的體積。
汽化
繼續對此液體加熱,分子運動的速度更快,分子距離的增加使分子力更形減弱。當分子運動的速度增快到可完全掙脫分子力的束縛時,液體就轉變成氣體,稱為汽化。
此時在液體內部形成許多氣泡翻湧而出,這種現象稱為沸騰。汽化後的氣體分子可以完全自由地移動,不受分子力的束縛,因此容易膨脹。由於氣體分子間的距離甚大,所以也容易被壓縮,這使得氣體沒有一定的形狀,也沒有一定的體積。
溫度與三態變化
|
一大氣壓下常見物質的熔點與沸點 |
|||||
|
物質 |
熔點(℃) |
沸點(℃) |
物質 |
熔點(℃) |
沸點(℃) |
|
鐵 |
1538 |
2861 |
水 |
0 |
100 |
|
銅 |
1085 |
2562 |
水銀 |
-39 |
357 |
|
金 |
1065 |
2856 |
酒精 |
-114 |
78 |
|
銀 |
962 |
2162 |
氮 |
-210 |
-196 |
|
鋁 |
660 |
2519 |
氧 |
-219 |
-183 |
|
鉛 |
327 |
1749 |
氦 |
- |
-269 |
|
根據由實驗測出的熔點或沸點,有助於我們判斷物質的種類。 |
|||||
在冰的熔化期間,由熱源處所輸入的熱能主要用於瓦解固體分子間的鍵結,而不是在增加分子運動的能量,(增加位能而不增加動能)因此冰在熔化時,溫度保持不變。每一克物質在熔化時,從固態轉變為同溫度的液態,所需吸收的熱量稱為該物質的熔化熱。由實驗可測知冰的熔化熱為80卡/克。
同理,在水的沸騰期間,由熱源處所輸入的熱能主要用於掙脫液體內分子間的束縛力,平均而言,分子運動的速度大小並沒有增加,因此氣態的水蒸汽和液態的水共存時,溫度不變。每一克物質在汽化時,從液態轉變為同溫度的氣態,所需吸收的熱量稱為該物質的汽化熱。由實驗可測知水在沸點時的汽化熱為540卡/克。
水或其他的純物質在冷卻降溫時,從「氣態→液態→固態」的變化過程,仍如圖所示,只是進行的方向相反而已。
氣體轉變成液體的現象,稱為液化。液化期間,氣態和液態共存,溫度保持不變。這時的溫度稱為凝結點。每一克物質在液化時,從氣態轉變為同溫度的液態,所需放出的熱量稱為該物質的凝結熱。在通常的狀況下,同一物質的凝結點和沸點相同;凝結熱和汽化熱相等。
同樣地,當液體受冷轉變成固體時,溫度保持不變,直至液體全部轉變成固體時為止。液體凝固期間的溫度稱為凝固點。在通常的狀況下,同一物質的凝固點和熔點相同;凝固熱和熔化熱相等。
潛熱
三種物態互變時,有一個現象值得注意,即當兩態互相轉換時,若末變為單一物態以前,用溫度計測量之,可發現其溫度會保持不變。此時可發現,熱能之進出,對溫度不生影響,此時能量並未消失,而是以另一種型式儲存起來。以每l克質量為準,其所吸入或放出之熱能稱為潛熱。水與冰互變之潛熱為80卡/克。水與水蒸氣間的潛熱則為539卡/克。
壓力對熔點、沸點的影響
壓力對物態之互變溫度有很大之影響。一般固體物質,熔解時體積增大,凝固時體積縮小,若外界大氣壓力增加,則熔解時體積不易增大,故熔點必升高。
少數固體,如冰、鑄鐵、銻、鉍等,熔解時體積縮小,凝固時體積增大,壓力增加熔點必降低。以冰為例,在1大氣壓之下,冰點(或熔點)為0℃,壓力大於1大氣壓時,冰點(或熔點)低於0℃,壓力小於1大氣壓時,冰點(或熔點)則高於0℃。
通常住於高山上或登山的人,常有水易沸騰而食物難熱之煮食經驗,這是因為高山之氣壓低,沸點也就不高,只要加上夠童之鍋蓋,或使用壓力鍋,調節一下壓力,軌可提高沸點,解決煮熟食物的問題。
例題3-6:
一質量30公克0℃的冰,加入100公克20℃的冷水,末溫為何?
0℃
想想看
1.何以在冰冷的天氣中,熱水反而比溫水容易結冰?
ANS:因為熱水汽化速度較快,因此溫度降低比溫水還快,故熱水反而比溫水易結冰。
2.
為何在降霜之前,在果樹上噴水,可防止水果凍傷?
ANS:在水果上噴水,可使水果減少與低溫環境直接接觸的面積。又當水凝固成冰時,反而會放出熱量使水果免於被凍傷。
水的三態變化和所伴隨的熱量進出,幾乎是處處可見。
◎廚房內作菜時,只要鍋內有水,不管鍋底下的火有多猛,就不必擔心菜會燒焦,因為水沸騰時,溫度保持不變。
◎裝熱水杯子的內側與裝冰水杯子的外側常見有小水珠,以及清晨時葉子上的小露珠,都是水蒸氣遇冷凝結成水的現象。
◎大雨前會覺得悶熱,這是因為空氣中的水蒸氣凝結,放出大量熱的緣故。
蒸發與昇華
液體因受熱而變成氣體之現象,稱為汽化。汽化又可分為蒸發與沸騰兩種。
蒸發
任何溫度下均有蒸發現象,它是位於液體表面之高速運動分子,逸出表面所造成,由於這種分子動能大,蒸發後所留下之分子動能比較小,因此它有降溫效果。
◎蒸發速率與物質種類及下列因素有關:即,溫度高、表面積大、表面附近空氣流速大、氣壓小或真空中都可得到高蒸發速率。
◎運動後(高溫),脫衣服(讓皮膚直接變成表面,表面積增大),再次電扇或冷氣之涼風(流速大),體溫容易降低而受涼。
◎地面上的一灘水,經一段時間後便不見了,就是蒸發所造成。
◎平常晾衣服可使衣服乾燥,也是蒸發的結果。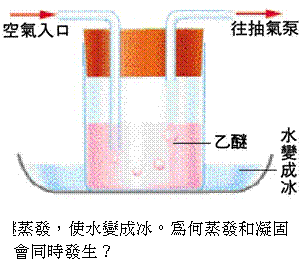
◎液體蒸發時,由於失去能量較大的分子,因此溫度會降低,造成冷卻的效果。
◎打針前,塗上酒精的手臂感覺涼快,便是因為酒精容易揮發,蒸發時溫度降低,再從手臂上吸熱所致。
◎沸騰與蒸發不同,它發生於液體內部,且在沸點時才會發生。
◎右圖顯示乙醚蒸發時吸熱,可使水結冰。
昇華
蒸發不一定只發生於液體,一些固體,如碘、乾冰(即固態二氧化碳)、樟腦等,可以直接受熱蒸發為氣態,此種過程稱為昇華。有昇華現象之物質,將其氣態冷卻也不經過液態,直接變為固體。
想想看
1.寒帶地區的人晾衣服,衣服先結冰變硬,過一段時間衣服便乾、變得柔軟,為何?
2.
冷氣機運轉時,常會有水排出,試問水從哪裡來?
ANS:冷氣機中低溫低溫的管子,會使空氣裡的水蒸氣凝結成水滴,所以當冷氣機運轉時,會持續地有水排出。